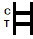Test szybkiego testu fibronektyny płodu
Użycie
Silny®Test PROM jest wizualnie interpretowanym testem immunochromatograficznym przeznaczonym do zastosowania do jakościowego wykrywania fibronektyny płodowej w wydzielaniach szyjki macicy. Obecność fibronektyny płodowej w wydzielinach szyjki macicy między 22 tygodnie, 0 dni i 34 tygodnie, 6 dni ciąży wynosizwiązane z podwyższonym ryzykiem porodu przedwczesnego.
Trodukcja
Dostawa przedwczesna, zdefiniowana przez American College of Obstetricians i Gynecologists jako dostawa przed 37. tygodniem ciąży, jest odpowiedzialna za większość niechromosomalnej zachorowalności i śmiertelności okołoporodowej. Objawy zagrożonej porodu przedwczesnego obejmują skurcze macicy, zmianę wydzieliny z pochwy, krwawienie z pochwy, ból pleców, dyskomfort brzuszny, ciśnienie miednicy i skurcze. Mody diagnostyczne do identyfikacji zagrożonej porodu przedwczesnego obejmują monitorowanie aktywności macicy i wydajność cyfrowego badania szyjnego, które pozwala na oszacowanie wymiarów szyjnych. Wykazano, że metody te są ograniczone, ponieważ minimalne rozszerzenie szyjki macicy (<3 centymetry) i aktywność macicy występuje normalnie i niekoniecznie diagnozują nieuchronne poród przedwczesny. Podczas gdy oceniono kilka markerów biochemicznych w surowicy, żaden nie został powszechnie przyjęty do praktycznego zastosowania klinicznego.
Fibronektyna płodu (FFN), izoforma fibronektyny, jest złożoną glikoproteiną adhezyjną o masie cząsteczkowej około 500 000 daltonów. Matsuura i współpracownicy opisali przeciwciało monoklonalne o nazwie FDC-6, które wyraźnie rozpoznaje III-CS, region definiujący izoformę płodową fibronektyny. Badania immunohistochemiczne łożyska wykazały, że FFN jestograniczone do macierzy pozakomórkowej regionu definiującego połączeniejednostek matczynych i płodowych w macicy.
Fibronektynę płodu można wykryć u wydzielania szyjki macicy kobiet przez całą ciążę za pomocą monoklonalnego testu immunologicznego przeciwciała. Fibronektyna płodu jest podwyższona w wydzielaniach szyjki macicy podczas wczesnej ciąży, ale jest zmniejszona z 22 do 35 tygodni w normalnych ciążach. Znaczenie jego obecności w pochwie we wczesnych tygodniach ciąży nie jest rozumiane. Może to jednak po prostu odzwierciedlać normalny wzrost pozbawionej populacji trofoblastów i łożyska. Wykrywanie FFN w wydzielinach szyjki macicy między 22 tygodnie, 0 dni a 34 tygodnie, 6 dni ciąży wiąże się z porodem przedwczesnym w objawowych i od 22 tygodni, 0 dni i 30 tygodniach, 6 dni u bezobjawowych kobiet w ciąży.
ZASADA
Silny®Test FFN wykorzystuje kolorową technologię immunochromatograficzną, przepływu kapilarnego. Procedura testowa wymaga solubilizacji FFN z wymazu pochwy poprzez zmieszanie wymazu w buforze próbki. Następnie mieszany bufor próbki dodaje się do dobrze próbki kasety testowej, a mieszanina migruje wzdłuż powierzchni membrany. Jeśli FFN jest obecny w próbce, utworzy kompleks z pierwotnym przeciwciałem anty-FFN skoniugowanym do kolorowych cząstek. Kompleks będzie następnie związany drugim przeciwciałem anty-FFN pokrytym błoną nitrocelulozą. Pojawienie się widzialnej linii testowej wraz z linią kontrolną wskazuje wynik dodatni.
Komponenty zestawu
| 20 Indywidualnie pAckurządzenia testowe ED | Każde urządzenie zawiera pasek z kolorowymi koniugatami i odczynnikami reaktywnymi wstępnie pokrytych w odpowiednich regionach. |
| 2EkstrakcjaFiolka buforowa | 0,1 M sól fizjologiczna buforowana fosforanem (PBS) i 0,02% azydka sodu. |
| 1 wymaz z kontroli pozytywnej (tylko na żądanie) | Zawierają FFN i azydkę sodu. Do kontroli zewnętrznej. |
| 1 wymaz kontroli negatywnej (tylko na żądanie) | Nie zawierają ffn. Do kontroli zewnętrznej. |
| 20 Rurki ekstrakcyjne | Do użycia przygotowania próbek. |
| 1 Stacja robocza | Miejsce do trzymania fiolek i rurek. |
| 1 Wkładka pakietu | Do instrukcji operacji. |
Materiały wymagane, ale nie dostarczone
| Regulator czasowy | Do użytku czasowego. |
ŚRODKI OSTROŻNOŚCI
■ Tylko dla profesjonalnego użycia diagnostycznego in vitro.
■ Nie używaj po dacie ważności wskazanej w pakiecie. Nie używaj testu, jeśli jego folia jest uszkodzona. Nie używaj ponownie testów.
■ Ten zestaw zawiera produkty pochodzenia zwierząt. Certyfikowana znajomość pochodzenia i/lub stanu sanitarnego zwierząt nie gwarantuje całkowicie braku przenoszonych środków patogennych. Zaleca się zatem, aby produkty te były traktowane jako potencjalnie zakaźne i obserwowane przestrzeganie zwykłych środków bezpieczeństwa (nie spożywaj ani nie wdychaj).
■ Unikaj zanieczyszczenia próbek za pomocą nowego pojemnika do zbierania próbki dla każdej uzyskanej próbki.
■ Ostrożnie przeczytaj całą procedurę przed wykonaniem wszelkich testów.
■ Nie jedz, nie pij ani nie palić w obszarze, w którym obsługiwane są okazy i zestawy. Obsługuj wszystkie okazy, jakby zawierały czynniki zakaźne. Zaobserwuj ustalone środki ostrożności związane z zagrożeniami mikrobiologicznymi w trakcie procedury i postępuj zgodnie ze standardowymi procedurami właściwego usuwania próbek. Noś odzież ochronną, taką jak płaszcze laboratoryjne, rękawice jednorazowe i ochrona oczu, gdy próbki są badane.
■ Nie wymieniają ani nie mieszaj odczynników z różnych działek. Nie mieszaj czapek butelek roztworu.
■ wilgotność i temperatura mogą niekorzystnie wpływać na wyniki.
■ Po zakończeniu procedury testowej starannie pozwól wymazom po autoklowaniu w 121 ° C przez co najmniej 20 minut. Alternatywnie można je leczyć 0,5% podchorowodorkiem sodu (lub wybielaczem domowym) przez godzinę przed usuwaniem. Zastosowane materiały testowe należy odrzucić zgodnie z przepisami lokalnymi, stanowymi i/lub federalnymi.
■ Nie używaj szczotek cytologii z pacjentami w ciąży.
Przechowywanie i stabilność
■ Zestaw powinien być przechowywany w 2-30 ° C, aż do wydrukowania na uszczelnionej torebce.
■ Test musi pozostać w uszczelnionej torebce do czasu użycia.
■ Nie zamrażaj.
■ Należy zachować troski w celu ochrony komponentów w tym zestawie przed zanieczyszczeniem. Nie używaj, jeśli istnieją dowody zanieczyszczenia drobnoustrojów lub opadów. Biologiczne zanieczyszczenie urządzeń dozujących, pojemników lub odczynników może prowadzić do fałszywych wyników.
Kolekcja i przechowywanie elektromenów
■ Używaj tylko sterylne wymazy Dacron lub Rayon z plastikowymi wałkami. Zaleca się skorzystanie z wymazu dostarczonego przez producenta zestawów (wymazy nie są zawarte w tym zestawie, aby uzyskać informacje o zamawianiu, skontaktuj się z producentem lub lokalnym dystrybutorem, numer katalogu wynosi 207000). Warzenia od innych dostawców nie zostały zatwierdzone. Nie zalecane są wymazy z bawełnianymi końcówkami lub drewnianymi szybami.
■ Wydzielania szyjki macicy są uzyskiwane z tylnej fornix pochwy. Proces zbierania ma być delikatny. Nie jest wymagana energiczna lub silna kolekcja, wspólna dla kultur mikrobiologicznych. Podczas badania spekulacyjnego, przed jakimkolwiek badaniem lub manipulacją szyjki macicy lub przewodu pochwy, lekko obróć końcówkę aplikatora przez tylną fornix pochwy przez około 10 sekund w celu wchłaniania wydzieliny szyjki macicy. Kolejne próby nasycenia końcówki aplikatora mogą unieważnić test. Usuń aplikator i wykonaj test zgodnie z zaleceniami poniżej.
■ Umieść wymaz do rurki ekstrakcyjnej, jeśli test może zostać natychmiast uruchomiony. Jeśli natychmiastowe testowanie nie jest możliwe, próbki pacjenta należy umieścić w suchej rurce transportowej do przechowywania lub transportu. Ważety można przechowywać przez 24 godziny w temperaturze pokojowej (15-30 ° C) lub 1 tydzień w 4 ° C lub nie więcej niż 6 miesięcy w -20 ° C. Wszystkie próbki powinny mieć możliwość osiągnięcia temperatury pokojowej 15-30 ° C przed badaniem.
PROCEDURA
Przed użyciem przenieś testy, próbki, bufor i/lub sterowanie do temperatury pokojowej (15-30 ° C).
■ Umieść czystą rurkę ekstrakcyjną w wyznaczonym obszarze stacji roboczej. Dodaj 1 ml buforu ekstrakcji do rurki ekstrakcji.
■ Włóż wymaz próbki do rurki. Energicznie wymieszaj roztwór, mocno obracając wymaz na bok rurki przez co najmniej dziesięć razy (podczas zanurzenia). Najlepsze wyniki uzyskuje się, gdy próbka jest energicznie mieszana w roztworze.
■ Wyciśnij jak najwięcej płynu z wymazu, uszczypując bok elastycznej rurki ekstrakcyjnej, gdy wymaz jest usuwany. Co najmniej 1/2 roztworu bufora próbki musi pozostać w rurce, aby wystąpić odpowiednia migracja kapilarna. Umieść czapkę na ekstrahowanej rurce.
Odrzuć wacik w odpowiednim biohazardowym pojemniku na odpady.
■ Wyodrębnione próbki mogą zatrzymać w temperaturze pokojowej przez 60 minut bez wpływu na wynik testu.
■ Wyjmij test z uszczelnionej torebki i umieść go na czystej, poziomej powierzchni. Oznacz urządzenie identyfikacją pacjenta lub kontroli. Aby uzyskać najlepszy wynik, test należy przeprowadzić w ciągu jednej godziny.
■ Dodaj 3 krople (około 100 µl) ekstrahowanej próbki z rurki ekstrakcyjnej do studni na próbce na kasecie testowej.
Unikaj pułapkowania pęcherzyków powietrza w studni (studni) i nie upuszczaj żadnego rozwiązania w oknie obserwacyjnym.
Gdy test zaczyna działać, zobaczysz, że kolor przesuwa się przez membranę.
■ Poczekaj, aż pojawią się kolorowe opaski. Wynik należy odczytać po 5 minutach. Nie interpretuj wyniku po 5 minutach.
Odrzuć zużyte rurki testowe i kasety testowe w odpowiednim biohazardowym pojemniku na odpady.
Nterpretacja wyników
| POZYTYWNYWYNIK:
| Na membranie pojawiają się dwa kolorowe pasma. Jeden pasmo pojawia się w regionie kontrolnym (C), a drugi pasmo pojawia się w regionie testowym (T). |
| NEGATYWNYWYNIK:
| Tylko jeden kolorowy pasek pojawia się w obszarze kontrolnym (c). W regionie testowym (T) nie pojawia się widoczna kolorowa pasmo. |
| NIEWAŻNYWYNIK:
| Pasmo kontrolne nie pojawia się. Wyniki każdego testu, który nie wytworzył pasma kontrolnego w określonym czasie czytania, należy odrzucić. Przejrzyj procedurę i powtórz z nowym testem. Jeśli problem będzie się utrzymywał, natychmiast zaprzestaj korzystania z zestawu i skontaktuj się z lokalnym dystrybutorem. |
NOTATKA:
1. Intensywność koloru w regionie testowym (t) może się różnić w zależności od stężenia celowanych substancji obecnych w próbce. Ale poziom substancji nie można ustalić za pomocą tego testu jakościowego.
2. Niewystarczająca objętość próbki, niepoprawna procedura działania lub wykonywanie wygaśnięć testów są najbardziej prawdopodobnymi przyczynami awarii pasma kontrolnego.
Kontrola jakości
■ Wewnętrzne kontrole proceduralne są zawarte w teście. Kolorowy pasek występujący w regionie kontrolnym (C) jest uważany za wewnętrzną pozytywną kontrolę proceduralną. Potwierdza wystarczającą objętość próbki i poprawną technikę proceduralną.
■ Zewnętrzne kontrole proceduralne mogą (tylko na żądanie) w zestawach, aby upewnić się, że testy działają prawidłowo. Ponadto kontrole mogą być użyte do wykazania prawidłowej wydajności przez operatora testowego. Aby wykonać test kontrolki dodatniej lub negatywnej, wypełnij kroki w sekcji procedury testowej, lecząc wymaz kontrolny w taki sam sposób jak wymaz próbki.
Ograniczenia testu
1. Ten test można wykorzystać wyłącznie do jakościowego wykrywania fibronektyny płodu w wydzielaniach szyjki macicy.
2. Wyniki testu powinny być zawsze stosowane w połączeniu z innymi danymi klinicznymi i laboratoryjnymi do zarządzania pacjentami.
3. Próbki należy uzyskać przed badaniem cyfrowym lub manipulacją szyjki macicy. Manipulacje szyjki macicy mogą prowadzić do fałszywie pozytywnych wyników.
4. Próbki nie należy zbierać, jeśli pacjent miał stosunek płciowy w ciągu 24 godzin, aby wyeliminować fałszywie pozytywne wyniki.
5. Pacjentów z podejrzeniem lub znanym zniekształceniem łożyska, łożysko previa lub umiarkowane lub rażące krwawienie z pochwy nie powinny być testowane.
6. Pacjenci z CERCLAGE nie powinni być testowani.
7. Charakterystyka wydajności silnej®Test FFN opiera się na badaniach kobiet z ciąży singleton. Wydajność nie została zweryfikowana u pacjentów z wieloma ciąży, np. Bliźniacy.
8. Silny®Test FFN nie ma być wykonywany w obecności pęknięcia błon owodniowych i pęknięcia błon owodniowych należy wykluczyć przed przeprowadzeniem testu.
Charakterystyka wydajności
Tabela: Test StrongStep® FFN vs. Test FFN Kolejna marki
| Względna wrażliwość: 97,96%(89,13%-99,95%)* Względna specyficzność: 98,73%(95,50%-99,85%)* Ogólna umowa: 98,55%(95,82%-99,70%)* *95% przedział ufności |
| Kolejna marka |
| ||
| + | - | Całkowity | |||
| Strongstep®FFn Test | + | 48 | 2 | 50 | |
| - | 1 | 156 | 157 | ||
|
| 49 | 158 | 207 | ||
Czułość analityczna
Najniższa wykrywalna ilość FFN w próbce wyodrębnionej wynosi 50 μg/l.
Wśród objawowych kobiet podwyższone poziomy (≥ 0,050 μg/ml) (1 x 10-7 mmol/l) FFN od 24 tygodni, 0 dni do 34 tygodni, 6 dni wskazuje na zwiększone ryzyko porodu w ≤ 7 lub ≤ 14 dni od od 14 dni od kolekcja próbek. Wśród kobiet bezobjawowych podwyższone poziomy FFN między 22 tygodnie, 0 dni a 30 tygodni, 6 dni wskazuje na zwiększone ryzyko porodu w ciągu ≤ 34 tygodni, 6 dni ciąży. Odcięcie 50 μg/L FFN ustalono w wieloośrodkowym badaniu przeprowadzonym w celu oceny związku między ekspresją fibronektyny płodu podczas ciąży a porodem przedwczesnym.
Zakłócające substancje
Należy zachować ostrożność, aby nie zanieczyszczać aplikatora lub wydzieliny szyjki macicy smarami, mydłem, środkami dezynfekującymi lub kremami. Smary lub kremy mogą fizycznie zakłócać wchłanianie próbki do aplikatora. Mydła lub dezynfekujące mogą zakłócać reakcję przeciwciała-antygenu.
Potencjalne zakłócające substancje badano przy stężeniach, które można rozsądnie znaleźć w wydzielaniach szyjki macicy. Poniższe substancje nie zakłócały testu po badaniu na wskazanych poziomach.
| Substancja | Stężenie | Substancja | Stężenie |
| Ampicylin | 1,47 mg/ml | Prostaglandin F2 | a0,033 mg/ml |
| Erytromycyna | 0,272 mg/ml | Prostaglandin E2 | 0,033 mg/ml |
| Mocz matki 3. trymestr | 5% (vol) | Monistatr (miconazol) | 0,5 mg/ml |
| Oksytocyna | 10 iu/ml | Indigo Carmine | 0,232 mg/ml |
| Terbutalin | 3,59 mg/ml | Gentamicyna | 0,849 mg/ml |
| Deksametazon | 2,50 mg/ml | Żel betadiner | 10 mg/ml |
| MGSO4• •7H2O | 1,49 mg/ml | Betadiner Cleanser | 10 mg/ml |
| Ritodryna | 0,33 mg/ml | K-oR galaretka | 62,5 mg/ml |
| Dermicidolr 2000 | 25,73 mg/ml |
Odniesienia do literatury
1. American College of Obstetricians and Gynecologists. Praca przedwczesna. Biuletyn techniczny, numer 133, październik 1989.
2. Creasy RK, Resnick R. Medycyna matczyna i płodu: zasady i praktyka. Filadelfia: WB Saunders; 1989.
3. Creasy RK, Merkatz IR. Zapobieganie porodowi przedwczesne: opinia kliniczna. Obstet Gynecol 1990; 76 (Suppl 1): 2s - 4s.
4. Morrison JC. Narodziny przedwczesne: zagadka warta rozwiązania. Obstet Gynecol 1990; 76 (Suppl 1): 5s-12s.
5. Lockwood CJ, Seniei AE, Dische MR, Casal DC i in. Fibronektyna płodu w wydzielinach szyjnych i pochwy jako predyktor porodu przedwczesnego. New Engl J Med 1991; 325: 669–74.
Glosariusz symboli
|
| Numer katalogowy |  | Ograniczenie temperatury |
 | Dotyczy instrukcji do użytku |
| Kod wsadowy |
 | Diagnostyczne urządzenie medyczne in vitro | 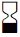 | Używać przez |
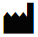 | Producent |  | Zawiera wystarczające dla |
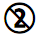 | Nie używaj ponownie |  | Upoważniony przedstawiciel w społeczności europejskiej |
 | CE oznaczony zgodnie z dyrektywą IVD Medical Devices 98/79/EC | ||
Liming Bio-Products Co., Ltd.
Nr 12 Huayuan Road, Nanjing, Jiangsu, 210042 PR Chiny.
Tel: (0086) 25 85476723 Faks: (0086) 25 85476387
E-mail:sales@limingbio.com
Strona internetowa: www.limingbio.com
www.stdiagnostics.com
www.stidiagnostics.com
Wellkang Ltd. (www.ce-marking.eu) tel: +44 (20) 79934346
29 Harley St., London Wig 9QR, UK Faks: +44 (20) 76811874
Szybkie urządzenie testowe Fibronectin Ferep®.

Dostawa przedwczesna, zdefiniowana przez American College of Obstetricians i Gynecologists jako dostawa przed 37. tygodniem ciąży, jest odpowiedzialna za większość niechromosomalnej zachorowalności i śmiertelności okołoporodowej. Objawy zagrożonej porodu przedwczesnego obejmują skurcze macicy, zmianę wydzieliny z pochwy, krwawienie z pochwy, ból pleców, dyskomfort brzuszny, ciśnienie miednicy i skurcze. Mody diagnostyczne do identyfikacji zagrożonej porodu przedwczesnego obejmują monitorowanie aktywności macicy i wydajność cyfrowego badania szyjnego, które pozwala na oszacowanie wymiarów szyjnych.
Szybki test fibronektyny Fłowej Strongstep® jest interpretowanym wizualnie testem immunochromatograficznym, który ma być stosowany do jakościowego wykrywania fibronektyny płodu w wydzielaniach szyjki macicy o następujących cechach:
Przyjazny dla użytkownika:procedura jednoetapowa w testach jakościowych
Szybki:Wymagane tylko 10 minut podczas odwiedzania tego samego pacjenta
Bez sprzętu:Szpitale ograniczające źródło lub warunki kliniczne mogą wykonać ten test
Dostarczony:temperatura pokojowa (2 ℃ -30 ℃)